Parowanie
Parowanie jest termodynamicznym procesem przechodzenia materii ze stanu ciekłego w stan lotny (gazowy).
Dla substancji proces ten zachodzi w różnych temperaturach. Na przykład pranie schnie nawet w niskich tempoeraturach.
Wrzenie jest to proces gwałtownego parowania, który przebiega w całej objętości cieczy. To właśnie wrzenie jest procesem, który zachodzi dla danej substancji w ścisle określonej temperaturze, przy stałym ciśnieniu. To tak zwana temperatura wrzenia.
Temperatura wrzenia wody
Temperatura wrzenia wody przy ciśnieniu równym 1 atm = 101 325 Pa wynosi 100°C. Temperatura ta przy określonym ciśnieniu stanowi temperaturę równowagi fazowej, w której faza gazowa i ciekła mogą istnieć jednocześnie.
Ciepło parowania
Ciepło parowania jest to iloraz ciepła \(Q\) potrzebnego do zmiany cieczy o masie m w gaz o tej samej temperaturze do tej masy \(m\).
gdzie:
- \(Q\) - dostarczane (lub oddawane) ciepło,
- \(m\) - masa ciała,
- \(c_p\) - ciepło parowania.
Jednostką ciepła parowania jest J/kg.
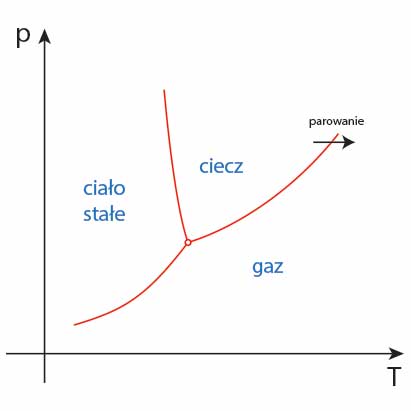
Parowanie na diagramie fazowym
Proces parowania uwidaczniamy na schematycznym diagramie fazowym za pomocą strzałki.
Ciecz przegrzana
Rozpoczęcie wrzenia jest uzależnione od obecności w cieczy tak zwanych zarodków wrzenia, na których rozpoczyna się proces gwałtownego parowania. To mogą być drobne zanieczyszczenia w cieczy. Brak takich zarodków prowadzi do tak zwanego przegrzania cieczy, która może osiągnąć temperaturę wyższą niż temperatura wrzenia. Aby przegrzać ciecz należy używać czystej chemicznie substancji, bardzo powoli podwyższać jej temperaturę i nie wywoływać żadnych wstrząsów. Drobne zaburzenie cieczy przegrzanej może spowodować gwałtowny i niebezpieczny dla eksperymentatora proces wrzenia.
Tablice
Oto temperatury wrzenia dla wybranych substancji:
| Substancja | Temperatura wrzenia [°C] |
|---|---|
| azot | -195,8 |
| cyna | 2610 |
| deuter | -249,5 |
| etan | -88,6 |
| etanol | 78,3 |
| gliceryna | 290 |
| glikol | 197,3 |
| kobalt | 3100 |
| krzem | 3280 |
| kwas mrówkowy | 100,7 |
| kwas octowy | 117,9 |
| kwas siarkowy | 274 |
| metan | -161,5 |
| miedź | 2570 |
| mocznik | 154 |
| ołów | 1756 |
| platyna | 4170 |
| pluton | 3300 |
| rtęć | 356,9 |
| siarka | 444,6 |
| srebro | 2155 |
| tlen | -182,96 |
| węglik hafnu | 5400 |
| woda | 100 |
Podane wartości dotyczą ciśnienia w warunkach normalnych (1 atm).

Pytania
Czy można doprowadzić do wrzenia substancję nie zmieniając jej temperatury?
Tak. Wynika to wprost z diagramu fazowego. Można czasem tylko poprzez zmianę ciśnienia bez zmiany temperatury również wywołać proces wrzenia.
© medianauka.pl, 2021-05-05, A-4049/2254
Data aktualizacji artykułu: 2025-04-23





