Przemiana izobaryczna
Przemiana izobaryczna lub proces izobaryczny to taka przemiana gazu, podczas której ciśnienie gazu \(p\) nie ulega zmianie (\(p=constans\)).
Prawo Gay-Lussaca
W przemianie izobarycznej stałej masy gazu doskonałego ciśnienie gazu nie ulega zmianie, zmieniają się natomiast temperatura i objętość gazu, a ich iloraz pozostaje stały.
W przemianie izobarycznej objętośc gazu jest wprost proporcjonalna do temperatury gazu. Im wyższa jest temperatura gazu, tym gaz bardziej zwiększa swoją objętość.
Przykład
Jeżeli mamy gaz zamknięty w cylindrze z ruchomym tłokiem i będziemy go powoli podgrzewać (zwiększać jego temperaturę), to automatycznie wzrośnie objętość gazu (tłok sam zacznie się przesuwać). Jeżeli dwa razy zwiększymy temperaturę, to dwa razy wzrośnie objętość.
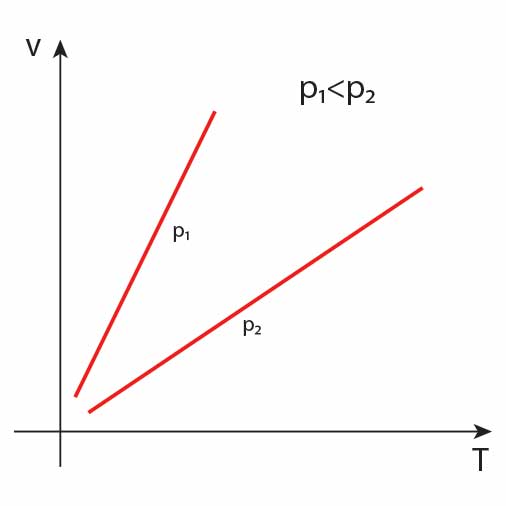
Izobara
Objętość gazu w przemianie izobarycznej jest wprost proporcjonalne do jego objętości, więc wykres zależności objętości od temperatury w przemianie izobarycznej to prosta - tak zwana izobara.
Wymiana ciepła podczas przemiany izobarycznej
Zgodnie z pierwszą zasadą termodynamiki \(\Delta U=W+Q\). Podczas przemiany izobarycznej temperatura gazu zmienia się i zmienia się zatem także energia wewnętrzna gazu. Zachodzi wymiana ciepła z otoczeniem.
Gdy mamy do czynienia z podgrzewaniem gazu, objętość gazu wzrasta i gaz wykonuje pewną pracę \(W\lt 0\). Wykonywana praca ma miejsce kosztem części ilości ciepła pobranego z otoczenia (\(Q\gt 0\)). Reszta ciepła jest zużywana na wzrost energii wewnętrznej gazu.
Gdy mamy do czynienia z ochładzaniem gazu (\(Q\lt 0\)), objętość gazu maleje i siły zewnętrzne wykonują wówczas pewną pracę nad gazem \(W\gt 0\), kosztem oddanego części ciepła.
© medianauka.pl, 2021-04-21, A-4029/2234
Data aktualizacji artykułu: 2025-04-23





